二氧化碳實(shí)驗(yàn)室制取方法
發(fā)布時(shí)間:2020-03-28 22:11:00
一、大理石與稀鹽酸反應(yīng)制取
1、口訣
實(shí)驗(yàn)室制二氧碳,大理石與稀鹽酸。兩種蘇打皆不用,速度太快控制難。
不用硫酸代鹽酸,鎂鹽不如鈣鹽廉。硝酸見(jiàn)光易分解,驗(yàn)滿(mǎn)瓶口火不燃。
2、反應(yīng)用品
大理石或石灰石(主要成分是CaCO?)和稀鹽酸。(實(shí)驗(yàn)室制二氧碳,大理石與稀鹽酸)
3、反應(yīng)原理-反應(yīng)方程式:
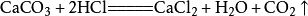
4、實(shí)驗(yàn)室二氧化碳制取裝置,固-液不加熱型(如圖)。
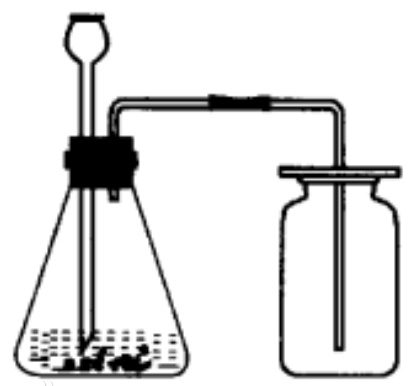
由于二氧化碳密度比空氣大,能溶于水且能與水反應(yīng),所以采用向上排空氣法。
6、檢驗(yàn)方法
將生成的氣體通入澄清的石灰水,石灰水變渾濁,證明該氣體為二氧化碳。
7、驗(yàn)滿(mǎn)方法
用燃著的木條被在集氣瓶口(不能伸入瓶?jī)?nèi)),如果火焰熄滅,證明已集滿(mǎn)。
8、注意事項(xiàng)
①反應(yīng)時(shí)可能揮發(fā)出的氯化氫(HCl)氣體,可通過(guò)飽和碳酸氫鈉(NaHCO3)溶液除去生成氣體中的氯化氫氣體。
②必要時(shí)可用裝有濃硫酸的洗氣瓶除去生成氣體中水蒸氣。
③不能用碳酸鈣和濃鹽酸反應(yīng),原因:濃鹽酸易揮發(fā)出大量氯化氫氣體,使碳酸氫鈉無(wú)法完全去除,制得的二氧化碳純度會(huì)下降。
④在實(shí)驗(yàn)室中是用大理石(CaCO?)和稀鹽酸反應(yīng)來(lái)制取二氧化碳。
⑤不能用Na?CO?(蘇打)和NaHCO?代替CaCO?(小蘇打)跟鹽酸反應(yīng)來(lái)制取二氧化碳,原因:Na?CO?和NaHCO?跟鹽酸反應(yīng)的速度太快,產(chǎn)生的二氧化碳很快逸出,不易控制,也不便于操作。(兩種蘇打皆不用,速度太快控制難)
⑥不能用稀硫酸代替鹽酸,原因:稀硫酸跟大理石(CaCO?)反應(yīng)會(huì)生成了微溶入水的硫酸鈣(CaSO?)沉淀覆蓋在大理石的表面上,阻礙了反應(yīng)的繼續(xù)進(jìn)行,而使反應(yīng)非常緩慢。(不用硫酸代鹽酸)
⑦不能用MgCO?(鎂鹽)代CaCO?(鈣鹽),原因:雖然MgCO?跟鹽酸與CaCO?跟鹽酸反應(yīng)相似,但由于MgCO?的來(lái)源較少,不如CaCO?廉價(jià)易得。(鎂鹽不如鈣鹽廉)
⑧不能用硝酸代替鹽酸,原因:硝酸見(jiàn)光易分解,方程式如下圖
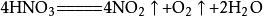
若用硝酸代替鹽酸,則制得的CO?中就會(huì)有少量的NO?和O?。此外,硝酸的價(jià)格較鹽酸貴,故通常不用硝酸代替鹽酸。(硝酸見(jiàn)光易分解)
⑨因?yàn)槎趸寄軠缁穑士梢詫⑷贾幕鸩裰糜诩瘹馄靠跈z驗(yàn),若火焰熄滅,則證明二氧化碳已經(jīng)充滿(mǎn)了集氣瓶。(鑒別火柴不能燃)
二、加熱使碳酸氫鈉分解制取
將碳酸氫鈉充分干燥后裝入硬質(zhì)玻璃管中,在管口處裝填玻璃棉后封閉,用抽氣泵抽真空。然后,加熱使碳酸氫鈉分解。最初發(fā)生的二氧化碳可放掉。分解產(chǎn)生的氣體需導(dǎo)入用冰冷卻的導(dǎo)管中,使氣體中的水蒸氣冷凝下來(lái),再將氣體先后導(dǎo)入分別裝有氯化鈣和五氧化二磷的U形管中使其干燥。100℃時(shí),碳酸氫鈉的分解壓為97.458kPa,120℃時(shí)為166.652kPa。
三、其他制法
小蘇打(主要成分是碳酸氫鈉)和白醋混合在一起時(shí),發(fā)生復(fù)分解反應(yīng),放出二氧化碳?xì)怏w,相應(yīng)的化學(xué)反應(yīng)方程式為: 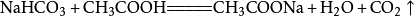
四、工業(yè)二氧化碳輸送設(shè)備
無(wú)錫市長(zhǎng)江高壓泵生產(chǎn)廠家二氧化碳泵適用于低溫液態(tài)二氧化碳的罐裝與輸送以及二氧化碳萃取加壓泵。可根據(jù)壓力流量選型。是用于啤酒、酒精制造廠及有關(guān)醫(yī)藥、食品工業(yè)的專(zhuān)用泵。二氧化碳泵造型美觀、維修方便、使用壽命長(zhǎng)。 


 當(dāng)前位置:
當(dāng)前位置: